银屑病(psoriasis)俗称“牛皮癣”,是一种由环境因素刺激、多基因遗传控制、免疫介导的皮肤病,典型表现为鳞屑性红斑或斑块,局限于一处或全身广泛分布。由于常迁延难愈,银屑病被称为“不死的癌症”,给患者造成身心、经济等重大负担。
在过去,传统药物虽能缓解患者症状,但仍面临着容易复发以及长期使用可能导致不良反应的困境。随着对银屑病发病机制的研究逐渐深入,许多新的作用靶点的药物不断出现,其中阿普米司特片作为我国首个获批的银屑病口服小分子靶向药物,兼顾持久疗效与良好安全性,给广大特殊人群与特殊部位的银屑病患者带来了治疗新思路。
阿普米司特片(曾用名:阿普斯特片)是一种磷酸二酯酶4(PDE4)小分子抑制剂。它可以通过抑制PDE4促使细胞内环磷酸腺苷(cAMP)含量升高,从而增加抗炎细胞因子,并下调炎症反应。
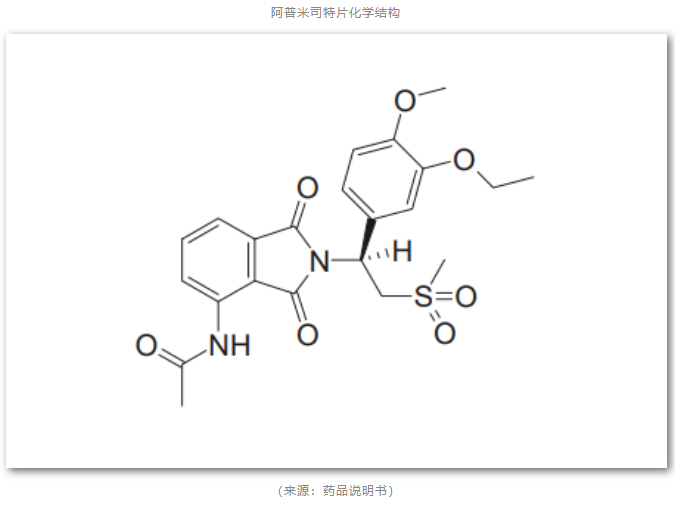
据了解,阿普米司特片最初由百时美施贵宝(BMS)旗下新基(Celgene)公司研发,2014年获FDA批准在美国上市(商品名:Otezla),目前在美国获批三个适应症:1)用于治疗成年活动性银屑病关节炎(PsA);2)中度至重度斑块型银屑病;3)与贝赫切特综合征(Behcet)相关的口腔溃疡。
2019年8月,安进宣布以高达134亿美元的价格获得阿普米司特,成功将其纳入麾下。
2021年2月,安进在中国提交阿普米司特上市申请并被纳入优先审评审批,同年8月获批进口,用于银屑病的治疗。
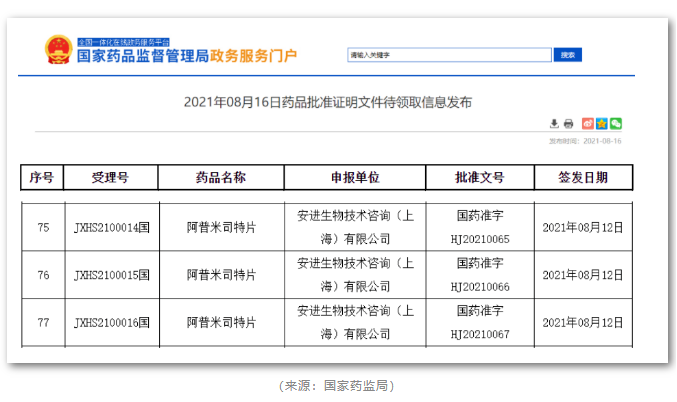
2023年01月18日,国家医保局正式公布了《国家基本医疗保险、工伤保险和生育保险药品目录(2022年)》,阿普米司特成功进入国家医保目录,进一步提升药品可及性,加速全球领先的创新药物惠及更多中国患者。
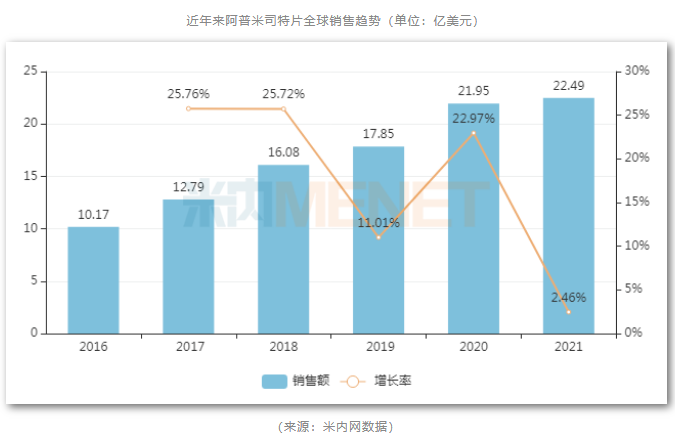
阿普米司特片自上市后,销售额一直稳步增长。根据安进2020年财报显示,这款产品全球销售额已经达到21.95亿美元。米内网数据显示,阿普米司特片2021年全球销售额达22.49亿美元,同比增长2.46%。
除此之外,阿普米司特还是过去20年中首个获批用于银屑病的口服药物,也是过去15年中首个获批用于PsA的口服药。这样的重磅品种自然引来国内企业的积极布局,但目前该产品尚无国内药企获批上市。业内人士分析,在接下来2-3年内阿普米司特的国产仿制药将迎来获批的井喷期,可以预见其竞争之激烈。
米内网数据显示,目前有超10家国内药企以新注册分类提交阿普米司特片上市申请,但多家药企的产品在首次申报时折戟成沙,终未获批。
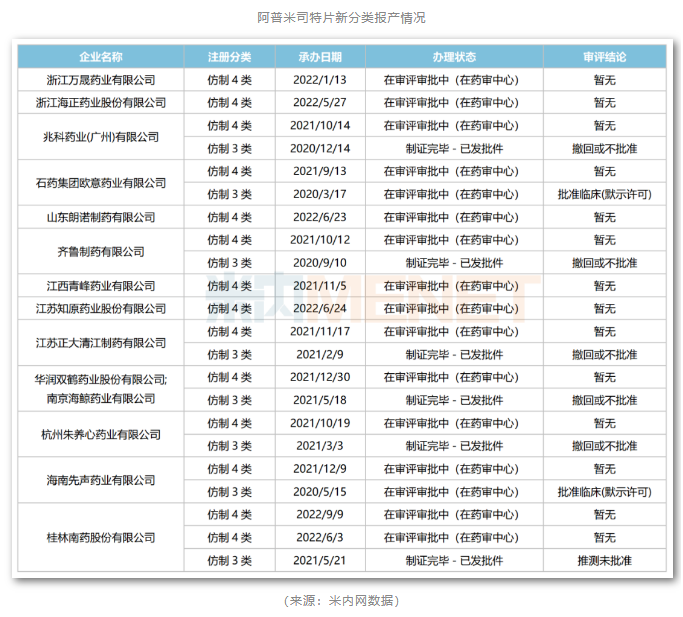
据米内网数据,从目前申报进度看,阿普米司特片首仿之争战况胶着,石药欧意的产品虽为首家,但齐鲁、兆科药业、杭州朱养心药业等企业也纷纷进入第一轮补充资料。那么,谁能突围抢到首仿呢?让我们拭目以待。



